Traitements thermiques des aciers
1. Mécanismes de refroidissement
1.1. Refroidissement d'un corps pur cristallin
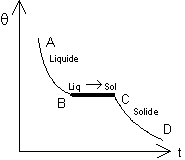
Sous une même pression constante, un corps pur cristallin, commence toujours à se solidifier ou à fondre à une même température s appelée température de solidification ou température de fusion (f). Les s et f sont égales et restent constantes pendant toute la durée de l'opération.
Remarque : La solidification d'un corps pur s'accompagne d'une diminution de volume appelé retrait, sauf pour quelques corps (eau, argent...) qui subissent une augmentation de volume.
1.2. Transformations allotropiques des corps purs cristallins

Il arrive, pour certains matériaux, que la courbe de refroidissement CD (phase solide) soit troublée par la présence d'un palier. La chaleur massique subit donc une variation entraînant une modification de la loi de refroidissement. Cette perturbation est la preuve d'une transformation profonde du corps pur. On l'appelle transformation allotropique. Les transformations allotropiques[1] se font à température constante.
Exemple : Quand on refroidit un échantillon de fer pur, il subit vers 906° la transformation suivante : Fer Fer .
Fer : mailles cubiques à faces centrées. Fer : mailles cubiques centrées.
Remarque : Les transformations allotropiques entraînent des variations de propriétés physiques (masse volumique, dilatabilité...).
1.3. Refroidissement d'un alliage binaire.
On appelle alliages binaires des substances métalliques formées de deux éléments chimiques. Ces alliages peuvent être homogènes[2] ou hétérogènes[3].
En général, un alliage binaire ne fond pas à température constante. Il existe donc un intervalle de fusion avec une température de début de fusion et une température de fin de fusion. Même chose pour la solidification.
Les alliages eutectiques[4] fondent et se solidifient à température constante.
1.3.1. Alliage binaire dont les deux métaux forment à froid une solution solide unique.
Examinons l'alliage Cu, Ni.
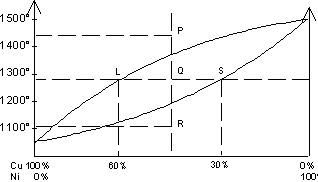
Étudions l'alliage à 50% de Cu et 50% de Ni.
P : L'alliage est entièrement liquide.
Q : 1260°, l'alliage est en cours de solidification. A cette température, la phase solide contient 30% de Cu et 70% de Ni et la phase liquide contient 60% de Cu et 40% de Ni.
R : L'alliage est entièrement à l'état solide.
1.3.2. Alliages binaires de métaux partiellement miscibles à l'état solide. Diagramme à point eutectique.
Nous nous bornerons dans ce paragraphe à étudier un diagramme à point eutectique à deux solutions solides.
On peut obtenir à partir de deux métaux A et B deux séries d'alliages homogènes de constitution différente. Les uns riches en A seront formés d'une solution solide (réseau cubique par exemple), les autres riches en B seront formés d'une solution solide (réseau hexagonal par exemple).

De A partent les branches liquidus, solidus correspondant à la solution solide .
De B partent les branches (liquidus, solidus) correspondant à la solution solide .
Les branches du liquidus se rejoignent en E : point eutectique et les branches du solidus rejoignent l'isotherme e en e1 (sol. sol.) et en e2 (sol. sol. ). Le solidus est donc constitué de trois parties : Ae1, e1e2 et e2B.
Cas de l'alliage eutectique : A température légèrement supérieure à 248,5 °C, l'alliage est encore liquide. A 248,5°C, il y a solidification à e = cste. Cette solidification s'opère par dépôt simultané de solution solide e1 et de solution solide e2. Pour connaître la teneur en chaque constituant de la phase solide, il suffit d'appliquer la règle des segments inverses.
sol.sol.e1 : X1 = ![]()
sol.sol.e2 : X2 =![]()
Cas des alliages homogènes : Ce sont ceux pour Pb% < 13% ou > 99%. Le refroidissement est analogue à celui des alliages binaires dont les deux métaux forment à froid une solution solide unique.
Cas des alliages hétérogènes : Ce sont ceux pour lesquels la teneur en Pb est comprise entre 13 et 99%.
- 13 à 87% : Il y a dépôt de sol.sol. jusqu'à la température e, à ce moment le dépôt de sol.sol. est à 13% de Pb. le reste étant à 87% de Pb, c'est de l'alliage eutectique qui se solidifie comme on l'a vu précédemment.
L'alliage est donc constitué de deux solutions : sol.sol.e1 et sol.sol.e2 et de deux constituants : sol.sol. pro eutectique et eutectique E d'où l'hétérogénéité.
- 87 à 99% : Même principe. On retrouve les deux mêmes solutions à savoir sol.sol.e1 et sol.sol.e2, mais cette fois les deux constituants sont le pro eutectique sol.sol. et l'eutectique E.
2. Diagrammes d'équilibre des alliages fer-carbone
2.1. Le fer
2.1.1. Propriétés :
= 7,86 f = s = 1528° HB = 80 Rm = 300MPa A% = 35 Il est ferromagnétique jusqu'à 728°C.
2.1.2. Structure cristalline et formes allotropiques :


Le fer cristallise dans un système cubique. Il existe deux sortes de mailles : maille cubique centrée et maille cubique à face centrée.
![]() : Atome de fer occupant le centre de la maille
ou des faces.
: Atome de fer occupant le centre de la maille
ou des faces.
![]() : Atome de fer occupant les sommets de la
maille.
: Atome de fer occupant les sommets de la
maille.
Fer : de 0 à 906°C. Réseau cristallin à maille cubique centrée. L'arête du cube mesure 2,87 pm.(1pm = 10-12m)
Fer : de 906 à 1401°C. La transformation du fer en fer se fait avec un apport de chaleur à température constante = 906°C. C'est un réseau à maille à faces centrées. L'arête du cube mesure 3,63 pm.
Fer : A partir de 1401°C le réseau cristallin redevient à mailles cubiques centrées. L'arête mesure 2,93 pm à 1425°C.
Conséquences : Il y a variation des propriétés physiques suivant la forme allotropique. En particulier on retiendra que c'est le fer qui est de loin le meilleur dissolvant du carbone.
2.2. Diagramme fer-carbone

Théoriquement, les aciers contiennent moins de 2.06% de C et les fontes de 2.06 à 6.67% de C. On admet que ces alliages sont binaires, les impuretés jouant un rôle négligeable dans les diagrammes d'équilibres.
On n'étudiera que le diagramme d'équilibre métastable fer-cémentite. La cémentite étant une combinaison chimique : Fe3C à 6,67% de C, qui est instable mais présente les apparences de la stabilité pour une importante plage de températures.
Le diagramme est quelque peu simplifié en ce sens que l'on n'a pas représenté ce qui concerne le fer : Toute petite région au-dessus de 1400°C avec une concentration en carbone < 0,07%.
Description du diagramme :
Les lignes :
· Liquidus : AC et CD
· Solidus : AE, ECF et FD
· Les lignes de transformation : GS, ES, GP, QP et PSK.
Les phases :
· Austénite : Solution solide de carbone dans le fer . Elle occupe à elle seule le domaine AESG.
· Ferrite : Solution solide de carbone dans le fer . Seule occupante du domaine GPQ, elle coexiste avec l'austénite dans GPS et avec la cémentite dans OPKR.
· Cémentite : Carbure de fer (Fe3C) à 6,67% de C. Elle coexiste avec l'austénite dans EFKS et avec la ferrite dans QPKR.
Points particuliers :
· Eutectique C : (4,3% de C) à 1145°C. Cet l'alliage est formé de cémentite et de sol.sol. de fer à 1,7% de C. L'eutectique C est appelé Lédéburite (52% de Fe3C et 48% d'austénite).
· Eutectoïde S : (0,85% de C) à 721°C. C'est un agrégat de ferrite et de cémentite. Cet eutectoïde est appelé Perlite ( 87,3% de ferrite et 12,7% de cémentite).
3. Traitements thermiques des aciers.
But : Faire varier les caractéristiques mécaniques du métal traité.
Principe : Un traitement thermique est une opération qui consiste à augmenter la température d'un métal, le maintenir à cette température et à le refroidir plus ou moins vite.
Les différents traitements thermiques : La trempe, le revenu, le recuit.
3.1. La trempe.
3.1.1. Mécanisme de la trempe.
On a vu lors de l'interprétation du diagramme fer-cémentite que si l'on pratique un refroidissement lent, l'austénite donne à température ambiante soit de la perlite + ferrite (0,2 à 0,85% de C), de la perlite seule (0,85% de C) ou de la perlite + cémentite (0,85 à 1,7% de C). Ce processus peur être totalement ou partiellement empêché selon la vitesse de refroidissement, il y a alors apparition de martensite ou de bainite.
Refroidissement rapide : Le refroidissement se faisant rapidement, les atomes de carbone en solution dans le fer n'ont pas le temps de diffuser, ce qui permettrait l'apparition de ferrite et de cémentite. Ils restent donc prisonniers dans le fer . Il y a apparition de martensite qui est une solution sursaturée de carbone dans le fer . Cette sursaturation provoque une déformation du réseau cristallin par cisaillement du réseau d'austénite. Il s'ensuit l'apparition de fortes contraintes qui produisent l'augmentation de la dureté. D'autre part, la sursaturation en carbone du fer produit des contraintes locales qui contribuent aussi à l'augmentation de la dureté.
Refroidissement intermédiaire : Quand la vitesse de refroidissement est intermédiaire, une certaine quantité de carbone qui serait en sursaturation dans le fer a le temps de s'échapper. Il y a donc formation de ferrite et de cémentite. Les constituants formés par le carbone dans le fer sont généralement appelés bainite. On parle de bainite supérieure, moyenne ou inférieure selon le degré de dureté.
La martensite est un constituant très dur, la bainite l'est un peu moins mais elle rend les matériaux moins fragiles.
3.1.2. Influence de la trempe.
La trempe augmente :
· la dureté (H),
· la résistance élastique (Re),
· la résistance maximale (Rm) à la traction.
La trempe diminue :
· la résilience (K),
· la striction (Z%)
· l'allongement % (A%).
3.1.3. Facteurs influençant les résultats.
Le pourcentage de carbone et les éléments d’addition : en dessous de
0,3% de C, les aciers sont peu sensibles à l’effet de la trempe. Certains
éléments d’addition comme le chrome, favorisent la pénétration de la trempe.

La température de trempe t : Elle présente un minimum : Ac3 + 50° (Ac3 = Ligne GS pour %C<0.85% ou = 721° pour %C0.85%) en dessous duquel la trempe ne peut avoir lieu. Il faut en effet que la ferrite soit transformée en austénite pour qu'au refroidissement, il y ait apparition de martensite ou de bainite.
La vitesse de refroidissement Vc : Elle présente elle aussi un minimum Vc (vitesse critique) en dessous duquel on n'obtient pas les transformations désirées. Ceci explique la variation de dureté entre l'extérieur et le cœur d'une pièce.
Le temps de maintien à t : Si ce temps est trop long, il risque de se produire deux choses : Un grossissement du grain et une décarburation superficielle de la pièce par dépôt de calamine, ceci rendant la trempe plus difficile.
3.1.4. Trempabilité.
L'expérience montre que si l'on trempe dans les mêmes conditions deux pièces semblables en dimensions et en composition chimique, on obtient en général des résultats différents. Ceci est dû à un comportement particulier de chaque acier qui ne dépend pas uniquement des dimensions et de la composition de l'échantillon mais aussi de facteurs dont les principaux sont la grosseur du grain, la présence d'inclusion (gaz, fines parcelles solides), les irrégularités de la composition chimique ou de la répartition des constituants et l'état de surface des pièces.
Courbes de trempabilité : La
trempabilité peut être représentée par une courbe donnant la dureté dans une
section transversale d'un barreau cylindrique de l'acier étudié en fonction de
sa distance au centre. La trempabilité doit être déterminée non pas une fois
pour chaque nuance d'acier, mais pour chaque coulée. L'établissement des
courbes de trempabilité étant très long, on a mis au point un essai très simple
permettant de définir la trempabilité d'un échantillon, c'est l'essai JOMINY.
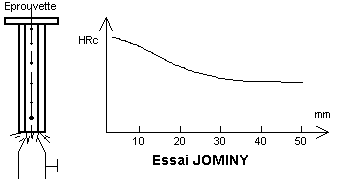
Essai Jominy : Cet essai consiste à projeter un jet d'eau froide sur l'extrémité inférieure d'une éprouvette cylindrique (L=100, D=25) portée à température de trempe pendant 30min et maintenue verticale, puis à mesurer la dureté HRC sur un méplat parallèle aux génératrices. La courbe jominy représente donc la dureté en fonction de la distance du point considéré par rapport à l'extrémité de l'éprouvette.
3.2. Trempe superficielle
3.2.1. Principe
La trempe superficielle consiste à chauffer localement la surface d’une pièce en acier jusqu’à la température d’austénitisation, à la refroidir rapidement pour obtenir un constituant de trempe en surface.
Le chauffage peut se faire par induction ou par flamme.
Le refroidissement se fait généralement par jet d’eau.
3.2.2. But
Obtenir une grande dureté en surface tout en conservant un bon allongement de la zone sous-jacente jusqu’au cœur de la section.
3.2.3. Intérêt
La grande dureté obtenue provient du refroidissement énergie venant de l’extérieur, mais aussi de l’intérieur de la pièce. Le volume de métal à refroidir est faible devant le volume de métal resté « froid ».
Pour obtenir la même dureté en surface par une trempe classique, il faut prendre des aciers fortement alliés, donc beaucoup plus chers.
3.2.4. Aciers utilisés
C42TS ou aciers faiblement alliés.
3.3. Le revenu.
Pour pratiquer un revenu sur un acier, il faut que celui-ci ait été préalablement trempé.
3.3.1. But du revenu.
Atténuer les contraintes créées par la trempe et obtenir pour des valeurs imposées de H, Rm, Re des valeurs plus élevées de A%, Z%, et K.
3.3.2. Mécanisme du revenu.
Un acier trempé est essentiellement composé de martensite et de bainite accompagné selon le type de trempe de cémentite, d'austénite résiduelle et de ferrite.
Le revenu consiste à élever la température de la pièce afin que les atomes de carbone retrouvent une certaine mobilité. Ceci peut provoquer différentes choses :
- La martensite libère quelques atomes de carbone et sa structure se rapproche progressivement de celle de la perlite.
- L'austénite non transformée poursuit sa transformation en martensite.
- L'austénite non transformée se transforme en cémentite.
3.3.3. Influence du revenu.
Diminution de : H, Re et Rm.
Augmentation de : Z%, A% et K.
Température de revenu et temps de maintien.
r doit toujours être inférieure à Ac1(Ligne de transformation correspondant à = 721°). Au début du traitement H décroît assez rapidement puis se stabilise. La durée de maintien à r ne joue plus au-dessus d'une certaine valeur.
Revenu de détente : r < 200°C. Rm , Re , Z% , H peu de variation.
Revenu banal ou classique : 500°C < r < Ac1. (K, A%, Z%) , (H, Rm, Re) .
Revenu de durcissement : 200°C < r < 600°C. Pour certains aciers seulement.
200°C < r < 300°C L'austénite résiduelle se transforme en bainite.
450°C < r < 600°C Précipitation de carbures très fins qui entraîne une augmentation de Rm, Re et H.
3.4. Le recuit.
3.4.1. Mécanisme.
Chauffage à rec > Ac3, maintien à cette température : l'austénite s'homogénéise. On fait un refroidissement lent donc on annule tout phénomène de trempe. Les constituants de l'acier refroidi sont alors la ferrite, la cémentite et la perlite.
Domaine d'application : Tout acier ayant subi des traitements antérieurs et/ou présentant une hétérogénéité. Chaque recuit a un but particulier. Le but du recuit n'est pas d'annuler l'effet de la trempe.
3.4.2. Les différents recuits.
Recuit de normalisation : rec = 900°, refroidissement air calme. Par convention, les caractéristiques mécaniques des aciers doivent être prélevés sur des échantillons normalisés.
Recuit de d'homogénéisation : rec = 200°. Ce recuit permet une homogénéisation par diffusion des éléments. Un lingot d'acier, par exemple, ne présente pas forcément une composition chimique uniforme (ségrégation majeure), il peut être alors souhaitable de lui faire ce type de recuit.
Recuit de régénération : rec = Ac3 + 75°. S'applique aux aciers ayant une structure relativement grossière (gros grains). C'est l'une des conséquences du recuit d'homogénéisation. Avec ce recuit, les gros grains se transforment en grains fins d'austénite qui donneront au refroidissement des grains fins de perlite, de ferrite ou de cémentite. Un maintien trop long à rec conduirait à un regrossissement du grain.
Recuit d'adoucissement : rec = Ac3 + 75° et refroidissement très lent. Ce recuit à pour objet d'obtenir un maximum d'usinabilité en faisant disparaître tous les constituants durs tels que martensite qui seront remplacé par de la ferrite et de la perlite. La forme lamellaire de la perlite favorise les opérations de fraisage et de perçage alors que la forme globulaire est préférable pour le tournage.
Recuit de stabilisation : 400° < rec < 600°. Il tend à faire disparaître les tensions internes provoqués par certains traitements tels que le forgeage, soudage.
Recuit de recristallisation : rec = Ac3 + 75°. Le travail à froid des aciers peut provoquer de l'écrouissage cause d'une grande fragilité, la structure cristalline est profondément déformée. C'est notamment le cas du laminage, étirage, tréfilage... Le but de ce recuit est donc de faire réapparaître une structure à grain correcte.
4. Traitements thermochimiques des aciers.
4.1. La cémentation.
But : Augmenter la teneur en carbone de la partie superficielle d'une pièce en acier à moins de 0,2% de carbone afin de pouvoir augmenter la dureté de cette partie en lui faisant subir une trempe.
Mécanisme de la cémentation : On introduit la pièce au sein d'un milieu susceptible de lui céder du carbone. Ce milieu peut être solide, liquide ou gazeux et porte le nom de cément. Les atomes de carbone libérés par le cément vont diffuser dans le métal. Pour que ceci se produise il faut chauffer la pièce au-dessus de Ac3 afin que le fer soit sous forme de fer qui absorbe bien le carbone.
Après la cémentation on fait subir une trempe à la pièce :
- soit en la laissant refroidir légèrement jusqu'à température de trempe (Ac3 + 50°) puis en la refroidissement rapidement : c'est la trempe différée. Elle entraîne peu de déformations.
- soit en faisant une retrempe qui consiste à
refroidir la pièce, puis la réchauffer à température de trempe et à effectuer
une trempe à l'eau ou à l'huile. On obtient de la martensite fine très dure.
Cément solide : Caron = 60% de charbon de bois + 40% de carbonate de baryum.
Céments liquides : Bains de sels fondus à base de cyanure et de carbonate de sodium...
Céments gazeux : gaz naturel, méthane, propane...
4.2. La nitruration
But : Augmenter la dureté de la couche superficielle d'une pièce par enrichissement en azote de cette couche superficielle. Il en résulte la formation d'une couche superficielle mince (0,1 mm environ) dont la dureté vickers peut atteindre 800 63 HRC.
L'accroissement de dureté obtenu est dû uniquement à l'augmentation de la teneur en azote du métal. Aucun traitement n'est nécessaire après nitruration contrairement à la cémentation.
Principe : Placer la pièce dans une atmosphère contenant du gaz d'ammoniac (NH3) à une température supérieure à 500°. On obtient alors la réaction suivante : 2 NH3 N2 + 3 H2. L'azote ainsi libéré se combine au fer pour former du nitrure de fer (Fe4N). Il s'ensuit une augmentation de dureté.
Cette augmentation n'est vraiment importante que si l'acier contient des éléments d'addition tels que le chrome ou l'aluminium, il y a dans ce cas formation de nitrures (NCr, NAl) qui sont des composants très durs.
Les pièces traitées doivent contenir au moins 0,3% de C. Un acier classique de nitruration contient 0,35% de C, 1,1% de Cr, 1 % d'Al et 0,2% de Mo.
4.3. Autres traitements
La carbonitruration : Elle consiste, pour les pièces contenant moins de
0,3% de C à augmenter la teneur en carbone et en azote de la zone superficielle
des pièces.
On fait séjourner les pièces
dans une atmosphère gazeuse (C3H8 pour le carbone, NH3
pour l'azote). On obtient alors une couche (0,1 mm) enrichie en azote et en
carbone et une couche sous-jacente (0,4 mm) enrichie en carbone seulement.
Après carbonitruration, il
faut faire une trempe à l'eau ou à l'huile.
La cyanuration : Augmentation de la teneur en azote et en carbone en
plongeant la pièce dans un bain de cyanure de sodium. Faire une trempe après
cyanuration.
La sulfinisation : C'est une cémentation par le soufre. Il n'y a pas
d'accroissement de dureté, mais le soufre confère à la pièce traitée une haute
résistance à l'usure.